Succinyl-coenzyme A
| Succinyl-coenzyme A | |
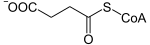 Structure de la succinyl-coenzyme A. | |
| Identification | |
|---|---|
| No CAS | 604-98-8 |
| No ECHA | 100.009.163 |
| PubChem | 92133 |
| ChEBI | 15380 |
| SMILES | CC(C)(COP(=O)(O)OP(=O)(O)OC[C@@H]1[C@H]([C@H]([C@@H](O1)N2C=NC3=C2N=CN=C3N)O)OP(=O)(O)O)[C@H](C(=O)NCCC(=O)NCCSC(=O)CCC(=O)O)O PubChem, vue 3D |
| InChI | InChI : vue 3D InChI=1/C25H40N7O19P3S/c1-25(2,20(38)23(39)28-6-5-14(33)27-7-8-55-16(36)4-3-15(34)35)10-48-54(45,46)51-53(43,44)47-9-13-19(50-52(40,41)42)18(37)24(49-13)32-12-31-17-21(26)29-11-30-22(17)32/h11-13,18-20,24,37-38H,3-10H2,1-2H3,(H,27,33)(H,28,39)(H,34,35)(H,43,44)(H,45,46)(H2,26,29,30)(H2,40,41,42)/t13-,18-,19-,20+,24-/m1/s1/f/h27-28,34,40-41,43,45H,26H2 InChIKey : VNOYUJKHFWYWIR-RIHFVUIRDN Std. InChI : vue 3D InChI=1S/C25H40N7O19P3S/c1-25(2,20(38)23(39)28-6-5-14(33)27-7-8-55-16(36)4-3-15(34)35)10-48-54(45,46)51-53(43,44)47-9-13-19(50-52(40,41)42)18(37)24(49-13)32-12-31-17-21(26)29-11-30-22(17)32/h11-13,18-20,24,37-38H,3-10H2,1-2H3,(H,27,33)(H,28,39)(H,34,35)(H,43,44)(H,45,46)(H2,26,29,30)(H2,40,41,42)/t13-,18-,19-,20+,24-/m1/s1 Std. InChIKey : VNOYUJKHFWYWIR-ITIYDSSPSA-N |
| Propriétés chimiques | |
| Formule | C25H40N7O19P3S [Isomères] |
| Masse molaire[1] | 867,607 ± 0,035 g/mol C 34,61 %, H 4,65 %, N 11,3 %, O 35,04 %, P 10,71 %, S 3,7 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
La succinyl-coenzyme A, usuellement abrégée en succinyl-CoA, est l'un des intermédiaires du Cycle de Krebs.
De l'α-cétoglutarate à la succinyl-CoA
La succinyl-CoA est issue de l'α-cétoglutarate par réduction de NAD+ et transfert sur la coenzyme A avec élimination d'une molécule de CO2. Le complexe alpha-cétoglutarate déshydrogénase catalyse cette réaction exergonique (ΔG° = −33 kJ/mol). L'énergie de cette réaction est stockée dans la liaison thioester de la succinyl-CoA. Ce complexe est très semblable au complexe pyruvate déshydrogénase et partage une origine commune. Cette réaction est irréversible.
De la succinyl-CoA au succinate
La succinyl-CoA permet la création de succinate en régénérant de la guanosine triphosphate (GTP) à partir de GDP et de phosphate inorganique Pi, et cela grâce à la liaison thioester à haut potentiel de transfert, c'est-à-dire qui possède une énergie libre d'hydrolyse très négative. Cette réaction permet aussi l'évacuation de la CoA-SH. La GTP pourra ensuite donner son phosphate à une ADP pour former de l'ATP. Cette réaction est catalysée par la succinyl-coenzyme A synthétase. Cette réaction est légèrement endergonique (ΔG° = 2,9 kJ/mol).
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
 Portail de la biochimie
Portail de la biochimie  Portail de la chimie
Portail de la chimie













